
題目列表(包括答案和解析)
| 元素編號 | a | b | c | d | e | f | g | h | i | j |
| 原子半徑/pm | 111 | 77 | 70 | 104 | 143 | 99 | 117 | 186 | 160 | 64 |
| 最高化合價(jià)或 最低化合價(jià) |
+2 | -4 | -3 | +6 | +3 | -1 | +4 | +1 | +2 | -1 |
| 主族 周期 |
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | ||||||||
| 2 | a a |
b b |
c c |
j j |
||||
| 3 | h h |
i i |
e e |
g g |
d d |
f f |
||
| ||
| ||
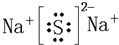
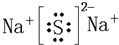


| 族周期 | ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | G | H | I | J | K |
 下表為部分短周期元素化合價(jià)及其相應(yīng)原子半徑的數(shù)據(jù).請回答下列問題:
下表為部分短周期元素化合價(jià)及其相應(yīng)原子半徑的數(shù)據(jù).請回答下列問題:| 元素性質(zhì) | 元素編號 | |||||||
| A | B | C | D | E | F | G | H | |
| 原子半徑(nm) | 0.102 | 0.117 | 0.074 | 0.110 | 0.071 | 0.075 | 0.077 | 0.099 |
| 最高化合價(jià) | +6 | +4 | +5 | +5 | +4 | +7 | ||
| 最低化合價(jià) | -2 | -4 | -2 | -3 | -1 | -3 | -4 | -1 |
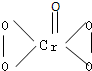 ?
?| a | b | ||||||||||||||||
| c | d | ||||||||||||||||
| e | f | g | h | ||||||||||||||
| i | j | ||||||||||||||||
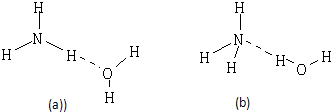
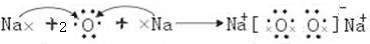
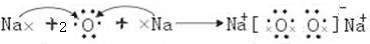
| A | |||||||||||||||||
| B | C | D | E | F | |||||||||||||
| G | H | I | J | ||||||||||||||
| K | M | L |





湖北省互聯(lián)網(wǎng)違法和不良信息舉報(bào)平臺 | 網(wǎng)上有害信息舉報(bào)專區(qū) | 電信詐騙舉報(bào)專區(qū) | 涉歷史虛無主義有害信息舉報(bào)專區(qū) | 涉企侵權(quán)舉報(bào)專區(qū)
違法和不良信息舉報(bào)電話:027-86699610 舉報(bào)郵箱:58377363@163.com