
題目列表(包括答案和解析)
| ||
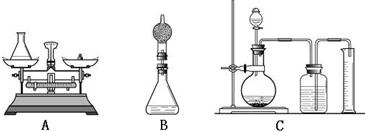
 Ti+2MgCl2.反應說明金屬鈦的活動性比鎂______(填“強”或“弱”).
Ti+2MgCl2.反應說明金屬鈦的活動性比鎂______(填“強”或“弱”).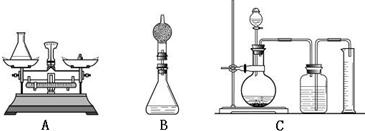
 Ti+2MgCl2.反應說明金屬鈦的活動性比鎂______(填“強”或“弱”).
Ti+2MgCl2.反應說明金屬鈦的活動性比鎂______(填“強”或“弱”).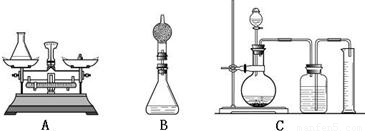
 Ti+2MgCl2.反應說明金屬鈦的活動性比鎂______(填“強”或“弱”).
Ti+2MgCl2.反應說明金屬鈦的活動性比鎂______(填“強”或“弱”).
| 加熱 |
| 實驗步驟 | 實驗現(xiàn)象 | 實驗結(jié)論 | |
| 實驗一 | 木條不復燃 | 常溫下過氧化氫溶液分解速度慢 | |
| 實驗二 | 在裝有過氧化氫溶液的試管中加入水泥塊,然后將帶火星的木條伸入試管中 | 木條復燃 |
湖北省互聯(lián)網(wǎng)違法和不良信息舉報平臺 | 網(wǎng)上有害信息舉報專區(qū) | 電信詐騙舉報專區(qū) | 涉歷史虛無主義有害信息舉報專區(qū) | 涉企侵權(quán)舉報專區(qū)
違法和不良信息舉報電話:027-86699610 舉報郵箱:58377363@163.com