
�}Ŀ�б�(�����𰸺ͽ���)
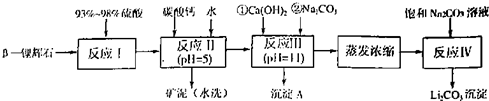
| �������� | Fe��OH��3 | Al��OH��3 | Mg��OH��2 |
| �_ʼ����pH | 2.7 | 3.7 | 9.6 |
| ��ȫ����pH | 3.7 | 4.7 | 11 |
| �ض�/�� | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3���ܽ��/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
| ��̖ | ���|(zh��) | �Y��ʽ | ˮ���ܽ��/g ��25�棩 |
���c/�� | ���c/�� |
| A | ��-�������� |  |
0.2 | 45 | 100 |
| B | ��-�������� | 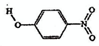 |
1.7 | 114 | 295 |
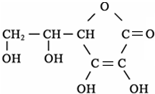 �������ʽ��
�������ʽ������ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙��e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com