
�}Ŀ�б�(�����𰸺ͽ���)
| �����}��ĴΔ�(sh��) | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
| ���������Q���|(zh��)���|(zh��)��/g | 78.9 | 97.8 | 116.7 | 135.60 | 155.05 | 175.05 | 195.05 |
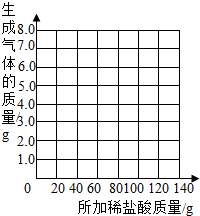
| ���ɚ��w���|(zh��)��/g | 1.1 | 2.2 | a | 4.4 | 4.95 | b | -- |
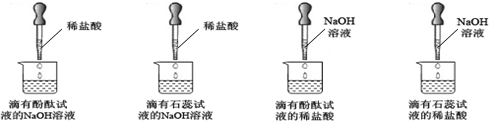
| ��ɫʯ��ԇҺ | pH��5.0���tɫ | 5.0��pH��8.0����ɫ | pH��8.0���{(l��n)ɫ |
| �oɫ��̪ԇҺ | pH��8.2���oɫ | 8.2��pH��10.0���tɫ | pH��10.0���oɫ |
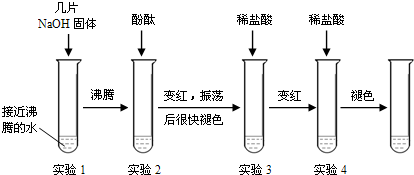
| �ض�/��C | 10 | 20 | 40 | 60 | 80 | 100 |
| �ܽ��/g | 64 | 85 | 138 | 203 | 285 | 376 |
| 106 |
| x |
| 73 |
| y?7.3% |
| 44 |
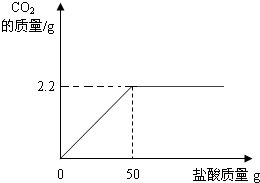
| 2.2g |
| 13.5g-5.3g |
| 13.5g |
| 106 |
| x |
| 73 |
| y?7.3% |
| 44 |
| 2.2g |
| 13.5g-5.3g |
| 13.5g |

�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com