
�}Ŀ�б�(�����𰸺ͽ���)
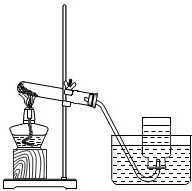 ̽���Ԍ������C���W(xu��)��Փ��һ�N��Ҫ��ʽ��Ҳչʾ�˻��W(xu��)�ğo�F������
̽���Ԍ������C���W(xu��)��Փ��һ�N��Ҫ��ʽ��Ҳչʾ�˻��W(xu��)�ğo�F������
| ||
| �� |
| ||
| �� |
| ||
| ||
| �������i |
| �������i |
�ٶ����� - ����(x��)���б� - ԇ�}�б�
����ʡ��(li��n)�W(w��ng)�`���Ͳ�����Ϣ�e��ƽ�_ | �W(w��ng)���к���Ϣ�e�^(q��) | ����p�_�e�^(q��) | ��vʷ̓�o���x�к���Ϣ�e�^(q��) | �����֙�(qu��n)�e�^(q��)
�`���Ͳ�����Ϣ�e���Ԓ��027-86699610 �e���]�䣺58377363@163.com